定义
药物性心脏毒性,是因外源性药物对心血管系统造成多种复杂的病理生理损害,临床表现为心肌炎、心肌病、心律失常、心瓣膜损害、心肌缺血及与心肌梗死等一系列心脏功能和器质性的改变。
心脏毒性可以发生在治疗期间,也可以发生在治疗后数月,甚至数年。
筛查时机
欧洲临床肿瘤学会(ESMO)在2020年发布的ESMO共识中有如下建议:
@在开始癌症治疗前检查心功能;
@在癌症治疗开始后每3个月对心功能进行一次随访;
如存在高风险因素,应咨询心脏病专家。肿瘤专家和心脏病专家之间的良好合作对于癌症治疗期间心血管毒性的管理至关重要。
癌症治疗相关心脏毒性的管理
引起心脏毒性的常见抗癌药物
蒽环类化疗药物
蒽环类药物包括阿霉素、表阿霉素、柔红霉素和阿克拉霉素等,是临床上最常用的、有效的抗肿瘤化疗药物之一。
广泛用于治疗血液系统恶性肿瘤和实体肿瘤,如急性白血病、淋巴瘤、乳腺癌,卵巢癌、膀胱癌、肺癌、甲状腺癌,胃癌,以及软组织肉瘤等。
蒽环类药物治疗的心肌损害过程

蒽环类药物引起的心脏毒性发病呈剂量依赖性。
当阿霉素剂量累积到400 mg/㎡时,3-5%的病人会出现心力衰竭;剂量累积到550 mg/㎡时发生率为7-26%,剂量累积到700 mg/㎡时发生率为18-48%。
除累积剂量外,还应密切关注以下情况:
65岁以上的老人、儿童、接受过胸部和纵隔放疗的患者、使用其他心脏毒性药物如曲妥珠单抗的患者、以及既往有心脏病史及并发症、心血管疾病风险(吸烟、高血压、糖尿病、血脂异常、肥胖)的患者,这类人群更容易发生心力衰竭。在此类人群中,应予以心脏病和心血管疾病风险的干预以防止心脏功能损伤。
蒽环类药物性心脏毒性的临床类型
蒽环类药物的心脏毒性分为急性心脏毒性,慢性(早期)心脏毒性,迟发性(慢性晚期)心脏毒性3个类别。
| 临床特征 | 急性心脏毒性 | 慢性心脏毒性 | |
| 早期 | 晚期 | ||
| 发作时间 | 蒽环类药物治疗开始治疗~治疗结束2周内 | 蒽环类药物治疗结束后1年内 | 蒽环类药物治疗结束1年后 |
| 剂量依存 | 不明 | 有 | 有 |
| 心脏超声 | 收缩功能减退 | 收缩功能减退 扩张心肌炎征象(室壁运动减弱更加明显) |
收缩功能减退 扩张型心肌炎征象(室壁运动减弱更加明显) |
| 过程 | 多数可逆 | 多数不可逆 收缩功能减退后马上开始心力衰竭治疗可逆 |
严重,难治性 |
心脏衰竭的进展阶段以及预防蒽环类药物性心肌病的时机
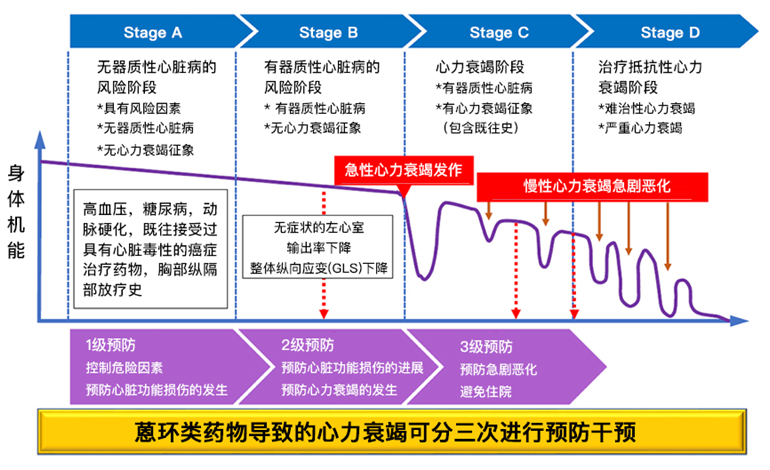
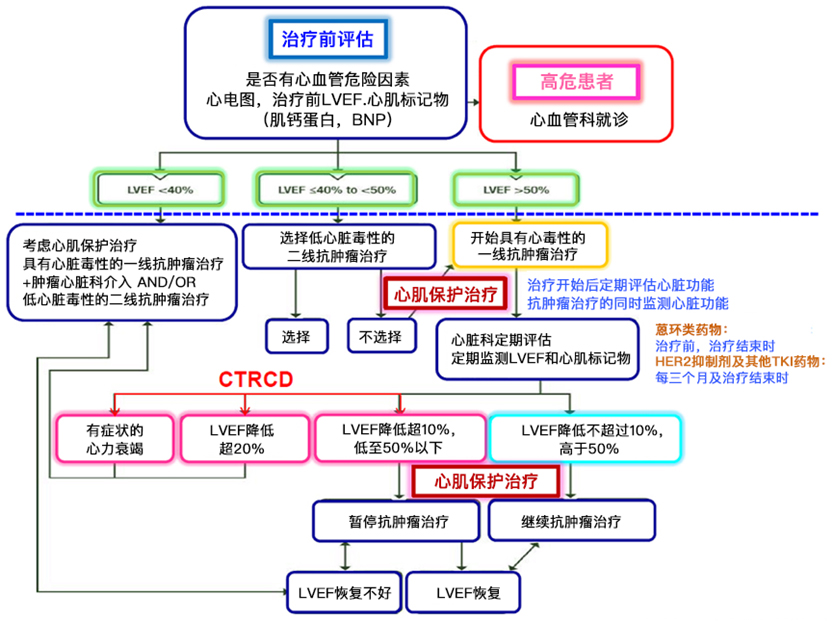
心脏毒性最初是发生在心肌细胞层面的损伤,继而引发心脏机能逐渐下降,最终破坏心脏代偿机制导致心力衰竭。
发生心力衰竭的患者,在给与蒽环类药物治疗后,血清肌钙蛋白会发生一过性增高,左心室射血分数(LVEF)下降。此时如果使用心脏保护药物治疗,大多数的患者LVEF会部分恢复,而一部分患者LVEF会恶化并出现心力衰竭。
研究者发现,9%的患者在接受蒽环类药物治疗后出现心脏毒性(LVEF <50%)。 而98%的心脏毒性发生在化疗结束后的1年内(中位数3.5个月))。使用依那普利和卡维地洛的治疗可以使82%的患者康复。
在无症状的心脏功能减退(stageB)患者中,心脏保护药物可以预防恶化,即可以预防心力衰竭。这就是为什么提早干预最有效的原因。然而,一旦错过了这个干预机会就会发生心力衰竭。这种不可逆的心肌损伤,治疗非常困难,可能会进入stageD。
早期发现的有效检查
@定期进行超声心动图检查
@测量肌钙蛋白
可被用来进行风险分级。
肌钙蛋白不升高的患者,随后出现心力衰竭的可能性较小,从而可减少超声心动图检查的频率。
肌钙蛋白水平升高和后续持续升高的患者更有可能发展为心力衰竭,可开始启用心脏保护药物的治疗,以及增加超声心电图的检查频率。
@监测BNP(B型钠尿肽)和NT-proBNP(N端脑钠肽前体)
BNP对LVEF<40%的心脏失代偿有很好的敏感性,但对LVEF在50%左右的患者则没有敏感性, 因此BNP可用于检测接近C期的B期晚期患者。
(对儿童和青少年癌症患者的蒽环类心肌病早期预测可能没有作用)
HER2抑制剂(靶向药物)
HER2抑制剂属于分子靶向药物,用于治疗HER2蛋白表达的癌症,特别是在乳腺癌的治疗中被广泛应用,胃癌治疗也有在使用。赫赫有名的曲妥珠单抗就是其中之一,还有帕妥珠单抗, 拉帕替尼, 以及新药T-DM1(抗体偶联药物ADC),DS8201(抗体偶联药物ADC)。
| 商品名 | 通用名 | 药物分类 |
|---|---|---|
| 赫赛汀 | 曲妥珠单抗 | 抗体药物 |
| 帕捷特 | 帕妥珠单抗 | 抗体药物 |
| 赫赛莱 | T-DM1 | 抗体偶联药物(ADC) |
| 泰立沙 | 拉帕替尼 | 酪氨酸激酶抑制剂(TKI) |
| ENHERTU | DS-8201 | 抗体偶联药物(ADC) |
HER2抑制剂心脏毒性的作用机制
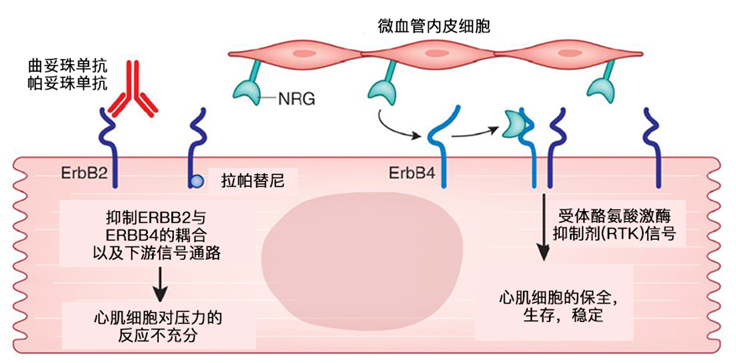
HER2抑制剂心脏毒性的危险因素
既往使用过蒽环类药物,有心力衰竭,高血压,缺血性心脏病史,接受过胸部放疗等情况,都会增加心脏毒性的风险。从表格中我们可以看出,心血管疾病的危险因素也是HER2抑制剂心脏毒性的重要危险因素。因此,常规的心血管疾病风险管理在药物性心脏毒性的管理中同样重要。
| 危险因素 | 风险等级 |
|---|---|
| 有心血管疾病史 | |
| 心功能障不全或心肌病 | 非常高 |
| 心肌梗死或做过冠状动脉搭桥手术 | 高 |
| 稳定性心绞痛 | 高 |
| 重症心脏瓣膜病 | 高 |
| 治疗前LVEF(左室射血分数)<50% | 高 |
| 治疗前LVEF(左室射血分数) 50~54% | 中② |
| 心律失常 | 中② |
| 心肌标记物 | |
| 治疗前肌钙蛋白异常 | 中② |
| 治疗前BNP或 NT-proBNP异常 | 中② |
| 心血管危险因素 | |
| 年龄≥80岁 | 高 |
| 年龄在65~79岁 | 中② |
| 高血压 | 中① |
| 糖尿病 | 中① |
| 慢性肾功能障碍 | 中① |
| 现阶段的抗肿瘤治疗 | |
| 蒽环类药物治疗后,接受HER2抑制剂治疗 | 中① |
| 同时接受蒽环类药物及HER2抑制剂治疗 | 高 |
| 既往抗肿瘤治疗中使用过心脏毒性药物 | |
| 接受过曲妥珠单抗的治疗 | 非常高 |
| 接受过蒽环类药物的治疗 | 中② |
| 左胸部或纵膈部位接受过放疗 | 中② |
| 生活习惯 | |
| 吸烟或曾经过度吸烟 | 中① |
| 肥胖(BMI>30kg/平方米 ) | 中① |
| 心脏毒性风险 | 风险等级 |
|---|---|
| 低危 | 无危险因素 或 有一个中等①的危险因素 |
| 中危 | 共计有2~4个中等危险因素 |
| 高危 | 共计有5个中等危险因素 或 有一个高等危险因素 |
| 极高危 | 具有1个以上超高危险因素 |
HER2抑制剂心脏毒性的特征和病程管理
HER2抑制剂引起的心脏毒性有一个特点,当左心室功能减退停用HER2抑制剂后,左心室功能通常会在2-4个月左右得到改善, 在LVEF恢复正常后即可考虑重新使用HER2抑制剂。但仍然有大约20-30%的患者心功能可能会持续恶化。
尽管停用HER2抑制剂,左心室功能可能会恢复,但在出现心脏毒性时,仍然建议使用ACE抑制剂(如依那普利)或β-受体阻滞剂(如Archest)予以心脏保护。
通常认为: 结合病人的具体情况,当左心室功能减退,肌钙蛋白升高、超声心动图显示功能减退,以及存在心血管危险因素的患者,需要进行长期的心脏保护性治疗。
靶向药物(VEGFR-TKI药物)
VEGFR-TKI,全称“血管内皮生长因子受体酪氨酸激酶抑制剂”,是小分子抗肿瘤血管生成的药物,也就是"血管生成抑制剂 "。它可以抑制酪氨酸激酶类受体(如VEGFR)磷酸化,因此被用于治疗各种癌症。
VEGFR-TKI药物的主要靶标以及适应症
| 通用名 | 英文名 | 靶标 | 适应症 |
|---|---|---|---|
| 索拉菲尼 | Sorafenib | VEGFR1-3 PDGFR c-KIT FLT-3 REF RAF |
肾细胞癌 肝细胞癌 甲状腺癌 |
| 舒尼替尼 | Sunitinib | VEGFR1-3 PDGFR c-KIT REF RAF |
肾细胞癌 GIST 胃肠道间质瘤 |
| 帕唑帕尼 | Votrient | VEGFR1-3 PDGFR c-KIT |
肾细胞癌 恶性软组织肿瘤 |
| 凡德他尼 | Vandetanib | VEGFR-2 EGFR RET |
甲状腺髓样癌 |
| 阿西替尼 | Axitinib | VEGFR1-3 PDGFR c-KIT |
肾细胞癌 |
| 瑞戈非尼 | Regorafenib | VEGFR1-3 PDGFR c-KIT TIE2 FGFR RET |
结直肠癌 胃肠道间质瘤 肝细胞癌 |
| 卡博替尼 | Cabozantinib | VEGFR2 MET RET c-KIT |
肾细胞癌 肝细胞癌 |
| 乐伐替尼 | Lenvatinib | VEGFR1-3 PDGFR c-KIT FGFR1 RET |
肾细胞癌 |
VEGFR-TKI药物的心脏毒性及危险因素
VEGFR-TKI 会导致高血压频发(15~40%),通常较多发生在开始治疗的头两个月内。另外,还观察到其他的心血管毒性,例如心肌损伤,心力衰竭(~5%),血栓栓塞(0.6-11.5%)和QT延长(0.6-13.4%)等。
除此之外,疲倦(35-50%)、腹泻(30-70%)、手足综合症等皮肤毒性(15~70%),肝功能损伤(5~50%)的发生频率也比较高。
VEGFR-TKI药物心脏毒性的管理
保持癌症治疗效果的同时,降低毒性风险是预防和治疗的根本。关于VEGFR-TKI药物心血管毒性的管理方法研究得很少,尚无特异性的管理方法。因此,常规的心血管风险管理非常重要。
高血压的治疗目标是早期诊断和控制血压。在开始VEGFR-TKI之前,应评估危险因素(如高血压病史和当前血压),并治疗现有高血压。开始治疗后,早期发现和治疗高血压可避免严重的并发症。就像通常治疗高血压一样,建议使用ACE抑制剂、ARB和二氢吡啶Ca拮抗剂)。 VEGFR-TKI通过CYP3A4代谢,因此应避免同时使用抑制CYP3A4的抗高血压药物(非二氢吡啶类Ca拮抗剂)。对于心功能减退的心力衰竭患者,ACE抑制剂、ARB和β-受体阻滞剂应是首选药物。
另外,VEGFR-TKI还会增加腹泻的频率,出现利尿剂导致的脱水风险。由于存在电解质异常和继发性QT间期延长的风险,应谨慎使用利尿剂。如果出现较严重的高血压,应与心脏病专家协作,共同监测和评估治疗效果,共同讨论VEGFR-TKI的治疗方案,减量,暂停或重启。
在治疗心力衰竭的过程中,应通过超声心动图定期进行评估,以便在心力衰竭症状出现之前早期发现心脏功能的恶化。如果是癌症治疗相关的心肌损害,可在心脏病专家的指导下开始使用肾素-血管紧张素抑制剂和β-受体阻滞剂。
在治疗血栓栓塞症时,如果提示血栓形成,如下肢水肿和D-二聚体升高,则通过下肢静脉超声评估深静脉血栓;如怀疑有肺栓塞,则进行胸部对比CT。当诊断为静脉血栓栓塞症时,为确定抗凝治疗的方法,要逐一评估出血和血栓形成的风险。对于肾功能正常的患者,推荐直接口服抗凝剂(DOACs),因为此类药物的出血风险比华法林低。 在出现心力衰竭或血栓栓塞时,肿瘤专家和心脏病专家应共同决定抗肿瘤治疗的方案。

图:基于抗血管生成抑制剂给药剂量/时间的血管毒性
免疫检查点抑制剂(ICI)
目前,有三种获批的ICI:抗PD-1、抗PD-L1和抗CTLA-4(表1)。适应症每年都在扩大,预计它们将成为继手术、化疗和放疗之后的第四种癌症治疗方法。
国内可使用的免疫检查点抑制剂药物
| 作用机制 | 通用名 | 商品名 | 适用症 |
|---|---|---|---|
| 抗PD-1抗体 | 纳武单抗 | 欧狄沃 | 黑色素瘤,非小细胞肺癌,肾细胞癌,霍奇金淋巴瘤,头颈部癌,胃癌,胸膜癌,MSI-H结直肠癌,食管癌 |
| 帕博利珠单抗 | 可瑞达 | 黑色素瘤,非小细胞肺癌,经典型霍奇金淋巴瘤,尿路上皮癌,MSI-H/dMMR实体瘤,肾细胞癌,头颈部癌 | |
| 抗PD-L1抗体 | 阿维鲁单抗 | 巴文西亚 | Merkel细胞癌,肾细胞癌,尿路上皮癌 |
| 阿替利珠单抗 | 阿特珠单抗 | 非小细胞肺癌,小细胞肺癌,肝细胞癌,乳腺癌(PD-L1阳性,非雌激素依赖性,HER2阴性) | |
| 度伐利尤单抗 | 英飞凡 | 非小细胞肺癌,小细胞肺癌 | |
| 抗CTLA-4抗体 | 伊匹木单抗 | 易普利 | 黑色素瘤,肾细胞癌,MSI-H/dMMR结直肠癌,非小细胞肺癌 |
免疫相关不良反应(irAE)
ICI对免疫系统的激活可能引起自身免疫性疾病。ICI的作用机制与传统的细胞毒性化疗药物和分子靶向药物不同,它引起的副作用被称为“免疫相关不良事件(irAE)”。可能发生在人体所有器官中,包括皮肤、消化系统、呼吸系统、内分泌系统和神经系统。
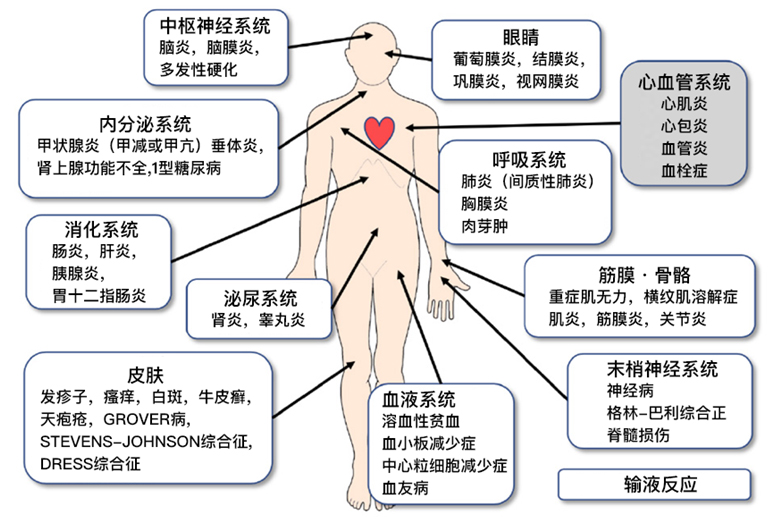
心脏中的irAE包括心肌炎、心肌病、心包病、心律失常等,其中心肌炎因其对预后的影响而最为重要。 心肌炎的发病率很低,约1%,但有些病例是暴发性的,报道称死亡率高达50%。因此,早发现早处理至关重要。ICI诱导的心肌炎的发病机制尚未明确,通常被认为是ICI抑制了心肌细胞上表达的PD-L1与T细胞上表达的PD-1的结合,导致了过度的免疫反应,或者也可能有一些其他机制。
irAE心肌炎的诊断
心肌炎没有特定的症状,患者可能完全没有感觉,而只是轻微的检验值异常;或者可能发展为暴发性心肌炎,出现突发性变化。 根据常见不良反应事件评价标准(CTCAE)5.0版,严重程度被分为5级。
心脏毒性的评估标准CTCAE
| Grade1 | Grade2 | Grade3 | Grade4 | Grade5 | |
|---|---|---|---|---|---|
| 心肠炎 | 无症状,有实验室检查,或心脏影像学正常 | 中度活动或劳累时出现症状 | 静息状态下或最低程度活动或劳累时变出现严重症状;需要治疗,新发症状 | 危机生命;需要紧急治疗(例如连续静脉输液治疗或机器辅助血液循环) | 死亡 |
在ICI治疗期间应定期监测生物标志物(肌钙蛋白、BNP)、心电图和超声心动图。通常,心肌炎在开始ICI治疗的3个月内最常见,因此在治疗的早期阶段应特别注意。90%以上的心肌炎患者会出现肌钙蛋白升高,但约一半的患者左心室收缩功能正常,所以超声心动图只是一种辅助诊断。
目前,心肌活检是诊断的金标准。组织病理学的特点是:细胞毒性T细胞(CD8+)、巨噬细胞(CD68+),辅助T细胞(CD4+)的浸润。不过它不是很敏感,而且很难与病毒性心肌炎相区别。而心脏MRI中的钆剂延迟增强核磁(LGE)和T2-STIR图像被证明有用,但与心肌活检一样,可能出现假阴性,应谨慎解释结果。 最终的诊断需要综合考虑这些影像所见。
ICI相关心肌炎的诊断
| 明确诊断心肌炎 *病理组织学检查 *心脏核磁共振所见 + 临床症状 +(生物标记物或心电图) *心脏超声所见(室壁运动异常)+ 临床症状 + 心电图 + 排除缺血性心脏病 |
| 疑似心肌炎 *心脏核磁共振所见(无 临床症状 + 生物标记物或心电图) 非特异性心脏核磁共振所见 + 临床症状/生物标记物/心电图中任意一个所见心肌炎 *心脏超声所见(室壁运动异常)+ 临床症状(心电图/生物标记物的任意一个) *PET 心脏所见+排除其他诊断 |
| 可能为心肌炎 *非特异性心脏核MRI所见(无 临床症状 + 生物标记物或心电图) *心脏超声所见(室壁运动异常)+ 临床症状或心电图 *生物标记物上升 + 临床症状或心电图所见 + 排除其他诊断 |
irAE心肌炎的治疗
如果患者的肌钙蛋白水平升高或心电图异常(Grade1),或有轻微症状(Grade2)时可暂停ICI治疗;
如果仅在停药后检测异常或症状有所改善,可以考虑重新启动ICI治疗,但目前没有足够的证据支持;
如果气短等症状加重(Grade2-3),在停用ICI后有必要予以糖皮质激素冲击治疗。原则上使用泼尼松龙1-2mg/kg;但如果病人的血液循环受到影响(Grade4),可给予糖皮质激素冲击治疗(甲基泼尼松龙1g/天),为期3天。
此外,在某些情况下可能需要心脏起搏器等机械循环支持;在糖皮质激素治疗无效时,有报告称,他克莫司、霉酚酸酯、英夫利西单抗、阿巴泰普等免疫抑制剂和大剂量免疫球蛋白可能有效,但缺乏证据。
